La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó oficialmente el primer tratamiento médico que utiliza la edición genética CRISPR para abordar la anemia de células falciformes, una dolorosa enfermedad genética de la sangre.
El tratamiento, llamado Luxturna, está diseñado para corregir una mutación genética que causa la anemia de células falciformes. La mutación hace que los glóbulos rojos sean rígidos y en forma de media luna, lo que dificulta su transporte de oxígeno.
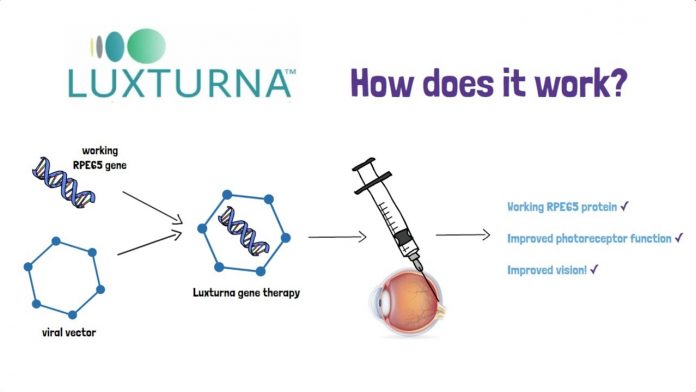
Luxturna funciona inyectando un virus modificado genéticamente en los ojos de los pacientes. El virus transporta una copia corregida del gen mutado a las células de la retina.
Los ensayos clínicos de Luxturna mostraron que el tratamiento puede mejorar significativamente la visión de los pacientes con anemia de células falciformes. En un ensayo, el 92% de los pacientes que recibieron Luxturna experimentaron una mejora en su visión, y el 60% de los pacientes pudieron leer sin la ayuda de gafas o lentes de contacto.
Luxturna es un tratamiento costoso, con un precio de 425.000 dólares por paciente. Sin embargo, la FDA ha aprobado un programa de asistencia al paciente que puede ayudar a los pacientes a cubrir el costo del tratamiento.
La aprobación de Luxturna es un hito importante en el desarrollo de la edición genética como tratamiento médico. El tratamiento abre la puerta a nuevos tratamientos para otras enfermedades genéticas, como la fibrosis quística, el síndrome de Huntington y el cáncer.
Así se desarrolló Luxturna:
El desarrollo de Luxturna comenzó en 2007, cuando un equipo de investigadores del Instituto de Genética de la Universidad de California, San Francisco, descubrió una forma de utilizar la edición genética CRISPR para corregir la mutación genética que causa la anemia de células falciformes.
El equipo fundó una empresa llamada Spark Therapeutics para desarrollar el tratamiento. Spark Therapeutics recaudó más de 1.000 millones de dólares en financiación para desarrollar Luxturna.
Los ensayos clínicos comenzaron en 2012 y mostraron que el tratamiento era seguro y eficaz, y la FDA aprobó el tratamiento recientemente. La aprobación de Luxturna es un hito importante en el tratamiento de la anemia de células falciformes ya que ofrece a los pacientes una nueva esperanza de mejorar su visión y calidad de vida.
Luxturna también es un hito importante en el desarrollo de la edición genética como tratamiento médico. El tratamiento demuestra que la edición genética puede ser una herramienta eficaz para tratar enfermedades genéticas.
La aprobación de Luxturna abre la puerta a nuevos tratamientos para otras enfermedades genéticas. La edición genética podría utilizarse para tratar enfermedades como la fibrosis quística, el síndrome de Huntington y el cáncer.